Hoá học 11 Bài 9: Axit nitric và muối nitrat
1.1.1. Cấu tạo phân tử
Hình 1: Công thức cấu tạo HNO3
Hình 2: Mô hình phân tử HNO3
-
Trong ptử HNO3: N có số oxi hóa là +5
1.1.2. Tính chất vật lí
- Axit nitric tinh khiết là chất lỏng, không màu, bốc khói mạnh trong không khí ẩm.
- Axit nitric kém bền. Ngay ở điều kiện thường, khi có ảnh sáng, dung dịch axit nitric bị phân hủy một phần giải phóng nitơ đioxit. Khí này tan trong dung dịch axit làm dung dịch có màu vàng.
Hình 3: Sự phân hủy HNO3 dưới tác dụng của ánh sáng
- Axit nitric tan trong nước ở bất kì tỉ lệ nào. Trong phòng thí nghiệm thường có loại HNO3 nồng độ 68%.
1.1.3. Tính chất hóa học
-
HNO3 phân li tạo H+ và NO3- ⇒ là axit mạnh
-
(Hmathop Nlimits^{ + 5} {O_3}) với N có số oxi hóa cao nhất ⇒ tính oxi hóa
Hình 4: N trong axit nitric nhận e thể hiện tính oxi hóa
Tính axit
HNO3 là axít mạnh
- Quỳ tím hoá đỏ
- Tác dụng với oxít bazơ, bazơ, muối của các axít yếu tạo muối nitrat.
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 +Ca(OH)2 → Ca(NO3)2+2H2O
2HNO3 + CaCO3 → Ca(NO3)2 + CO2 + H2O
- Các em chú ý quan sát thí nghiệm sau đây:
Video 1: phản ứng giữa Na2CO3 và HNO3
- Hiện tượng: Bột Na2CO3 tan ra. xuất hiện khí không màu
- Giải thích: Phản ứng giữa Na2CO3 và HNO3 diễn ra, tạo khí không màu là CO2
Tính oxi hoá
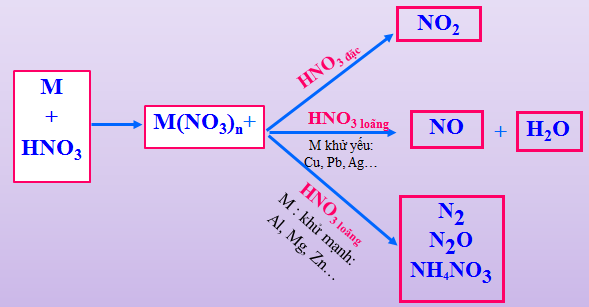
HNO3 có số oxi hóa +5 có thể bị khử thành: (mathop {{N_2}}limits^0 ,{rm{ }}mathop {{N_2}}limits^{ + 1} O,{rm{ }}mathop Nlimits^{ + 2} O,{rm{ }}mathop Nlimits^{ + 4} {O_2},{rm{ }}mathop Nlimits^{ - 3} {H_4}mathop Nlimits^{ + 5} {O_3})tuỳ theo nồng độ HNO3 và khả năng khử của chất tham gia.
Tác dụng với kim loại
Hình 5: Các sản phẩm khử của HNO3
Với M là kim loại, n là hóa trị cao nhất của M
*Lưu ý:
N2O là khí vui, khí gây cười.
N2 không duy trì sự sống, sự cháy
NH4NO3 không sinh ra ở dạng khí, nhưng khi cho kiềm vào dd, thấy có khí mùi khai.
- Oxi hoá hầu hết kim loại (trừ Au, Pt).
3Cu +8HNO3(l) → 3Cu(NO3)2 + 2NO + 4H2O
Cu + 4HNO3đ → Cu(NO3)2 + 2NO2 + 2H2O
- Fe, Al, Cr thụ động hoá với HNO3 đặc, nguội.
- Các em chú ý quan sát các thí nghiệm sau đây:
Video 2: Phản ứng của đồng tiền (Đồng) và axit nitric
- Hiện tượng: Đồng tiền với chất liệu bằng đồng tan ra, sủi bọt khí không màu, sau đó hóa nâu trong không khí, dung dịch chuyển thành màu xanh
- Giải thích: Đồng phản ứng với dung dịch axit nitric tạo dung dịch Cu2+ có màu xanh đặc trưng, thoát ra khí NO, khí NO phản ứng với oxi không khí tạo ra NO2 có màu nâu đỏ.
Tác dụng với phi kim
HNO3 đặc, nóng oxi hóa được một số phi kim C,S,P,... tạo NO2
(begin{array}{l} mathop Climits^0 + 4Hmathop Nlimits^{ + 5} {O_3} to mathop Climits^{ + 4} {O_2} + 4mathop Nlimits^{ + 4} {O_2} + 2{H_2}O mathop Slimits^0 + Hmathop Nlimits^{ + 5} {O_3} to {H_2}mathop Slimits^{ + 6} {O_4} + 6mathop Nlimits^{ + 4} {O_2} + 2{H_2}O end{array})
Video 3: Phản ứng giữa HNO3 và S
- Hiện tượng: Bột lưu huỳnh tan ra một phần, có khí thoát ra. Khi thử dung dịch tạo thành bằng dung dịch BaCl2 thấy có kết tủa trắng
- Giải thích: HNO3 phản ứng với S tạo khí NO2. Sản phẩm tạo thành có chứa H2SO4 nên khi thử dung dịch bằng BaCl2 thấy có kết tủa trắng BaSO4
Tác dụng với hợp chất
- HNO3 đặc oxi hoá nhiều hợp chất vô cơ và hữu cơ
(mathop {Fe}limits^{ + 2} O + Hmathop Nlimits^{ + 5} {O_3} to mathop {Fe}limits^{ + 3} {(N{O_3})_3} + mathop Nlimits^{ + 4} {O_2} + 2{H_2}O)
- Vải, giấy, mùn cưa, dầu thông….bị phá huỷ khi tiếp xúc HNO3 đặc
1.1.4. Ứng dụng
Hình 5: Ứng dụng axit nitric và muối nitrat
1.1.5. Điều chế
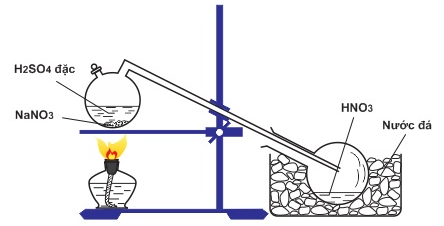
Trong phòng thí nghiệm
Cho tinh thể NaNO3 (hoặc KNO3) tác dụng với H2SO4 đặc, đun nóng
NaNO3 + H2SO4(đ) HNO3 + NaHSO4
Hình 6: Điều chế HNO3 trong phòng thí nghiệm
Trong Công nghiệp
Sản xuất HNO3 từ NH3, không khí: Gồm 3 giai đoạn
- Oxi hoá khí NH3 bằng oxi kk thành NO:
4NH3+ 5O24NO +6H2O (triangle H < 0)
- Oxi hoá NO thành NO2 bằng oxi kk ở điều kiện thường :
2NO + O2 → 2NO2
- NO2 tác dụng với nước và oxi không khí tạo HNO3:
4NO2 + O2 + 2H2O → 4HNO3
Dung dịch HNO3 có nồng độ 52 - 68 %
→ Để HNO3 có nồng độ cao hơn: Chưng cất với H2SO4 đậm đặc.
1.2.1. Tính chất của muối nitrat
Tính chất vật lý
Tất cả các muối nitrat đều tan trong nước và là chất điện li mạnh.
Ca(NO3)2 → Ca 2+ + 2NO3-
KNO3 → K+ + NO3-
Tính chất hoá học
Các muối nitrat đều kém bền bởi nhiệt, khi đun nóng muối nitrat có tính OXH mạnh.
Sản phẩm phân huỷ phụ thuộc vào bản chất của cation kim loại:
- Kim loại đứng trước Mg muối Nitrit + O2
Ví dụ: 2KNO3 2KNO2 + O2
-
Từ Mg đến Cu Oxit kim loại + NO2 + O2
Ví dụ: 2Cu(NO3)2 2CuO + 4NO2 + O2
-
Kim loại sau Cu Kim loại + NO2 + O2
Ví dụ: 2AgNO3 2Ag + 2NO2 + O2
1.2.2. Ứng dụng của muối nitrat
- Phân đạm trong nông nghiệp như NH4NO3, NaNO3, KNO3, Ca(NO3)2, ...
- Kali nitrat còn được sử dụng làm thuốc nổ đen (thuốc nổ có khói)
Hình 7: Chu trình của Nitơ trong tự nhiên
(1). Cây xanh đồng hóa nitơ chủ yếu ở dạng muối nitrat và muối amoni, chuyển hóa thành protein thực vật. Động vật đồng hóa protein thực vật, tạo ra protein động vật. Các chất hữu cơ do động vật bài tiết ra (phân, nước tiểu,...) cũng như xác động vật lại chuyển thành hợp chất hữu cơ chứa nitơ. Nhờ những loại vi khuẩn khác nhau có trong đất, một phần các hợp chất này chuyển hóa thành amoniac, rồi thành muối nitrat, phần còn lại thoát ra ở dạng nitơ tự do bay vào khí quyển. Khi các chất hữu cơ (than gỗ, than đá, than bùn,...) bị đốt cháy, nitơ tự do cũng được thoát ra. (2). Trên thực tế, có một số quá trình tự nhiên cho phép bù lại một phần lượng nitơ bị mất.
- Trong mưa giông, khi có sự phóng điện do sấm sét một phần nitơ tự do trong khí quyển kết hợp với oxi tạo thành khí NO, rồi chuyển hóa thành HNO3 và theo nước mưa thấm vào đất. HNO3 chuyển thành muối nitrat khi kết hợp với muối cacbonat, thí dụ canxi cacbonat có trong đất.
- Một số loại vi khuẩn, đặc biệt là các vi khuẩn cố định đạm sống ở rễ cây họ đậu có khả năng hấp thụ nitơ từ khí quyển và chuyển hóa thành các hợp chất chứa nitơ.
(3). Để tăng năng suất mùa màng, lượng nitơ chuyển từ khí quyển vào đất vẫn không thể đủ. Người ta ước tính lượng nitrat tái sinh tự nhiên chỉ bằng một nửa lượng nitrat bị hấp thụ. Do đó, cần phải bón vào đất những hợp chất chứa nitơ dưới dạng các loại phân bón hữu cơ và vô cơ.
Link nội dung: https://chodichvu.vn/bai-9-hoa-11-a53239.html